El Calor y la Temperatura vs Calor
Calor
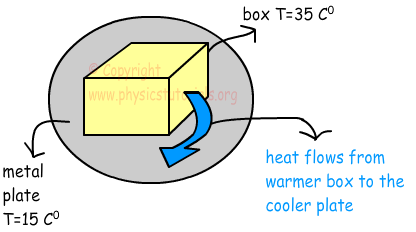
El calor es una forma de energía que fluye de la sustancia más caliente a más frío. Se entiende por sustancia más caliente y más frío, sustancia que tiene la temperatura alta y baja temperatura con respecto a un asunto de referencia.
 Debe haber una diferencia de temperatura de la sustancia que el calor o la transferencia de energía. El calor se relaciona con la cantidad de materia también. Si el objeto tiene una masa grande que también tiene gran energía térmica y por lo tanto aumenta la cantidad de energía transferida. Ya que es un tipo de energía que utilizamos Joule o calorías como unidad de calor.
Debe haber una diferencia de temperatura de la sustancia que el calor o la transferencia de energía. El calor se relaciona con la cantidad de materia también. Si el objeto tiene una masa grande que también tiene gran energía térmica y por lo tanto aumenta la cantidad de energía transferida. Ya que es un tipo de energía que utilizamos Joule o calorías como unidad de calor.
 Las diferencias entre calor y temperatura
Las diferencias entre calor y temperatura
En la vida diaria la mayoría de nosotros usamos estos términos indistintamente. En esta sección nos enteramos de las diferencias entre ellos.
El calor es un tipo de energía, pero la temperatura no es energía.
El calor depende de la masa de la sustancia, sin embargo, la temperatura no depende de la cantidad de materia. Por ejemplo, la temperatura de un vaso de agua hirviendo y una tetera de agua hirviendo son iguales entre sí, por el contrario tienen calor diferente, ya que tienen diferentes masas.
Usted puede medir la temperatura directamente con un dispositivo llamado termómetro, pero el calor no se puede medir con un dispositivo directamente. Usted debe saber la masa, temperatura y calor específico de la materia.
Si usted le da calor a un asunto, se aumenta su temperatura o cambiar su fase.
Capacidad de calor específico
Si le das la misma cantidad de calor a diferentes tipos de materia se observa que los cambios en las temperaturas son diferentes. Por ejemplo, todo lo que la experiencia que da la misma cantidad de calor para cucharas de metal y cucharas de madera, cuchara de metal tiene un mayor cambio en su temperatura. Por lo tanto, la mayoría de las amas de casa usan cucharas de madera o de plástico mientras se cocina.
 Estos ejemplos muestran que cada materia tiene sus propias características para absorber el calor. Llamamos a este concepto como la capacidad de calor específico de la materia. Es la propiedad que la distingue de la materia. Lo demostramos con la letra “c” y dar la definición de lo que, el calor necesario para aumentar la temperatura de la masa de la unidad 1ºC. Por el contrario, la capacidad calorífica del sistema se define como “el calor necesario aumentar la temperatura de la sustancia entera” y nos muestran con “C”.
Estos ejemplos muestran que cada materia tiene sus propias características para absorber el calor. Llamamos a este concepto como la capacidad de calor específico de la materia. Es la propiedad que la distingue de la materia. Lo demostramos con la letra “c” y dar la definición de lo que, el calor necesario para aumentar la temperatura de la masa de la unidad 1ºC. Por el contrario, la capacidad calorífica del sistema se define como “el calor necesario aumentar la temperatura de la sustancia entera” y nos muestran con “C”.
C=m.c donde m es la masa de la sustancia y c es el calor específico de la materia.
Con la ayuda de calor específico y la masa de la materia que se puede encontrar la relación entre el calor y el cambio en la temperatura de la fórmula que figura a continuación.
Q=m.c.∆T
Donde, Q es el calor, m es la masa, c es la capacidad de calor específico y la ΔT es el cambio en la temperatura.
El Calor, la Temperatura y la Expansión Térmica Exámenes y Soluciones