Cálculo de Transferencia de Calor
Los cálculos de transferencia de calor
La conservación del teorema de la energía también se aplica a la transferencia de calor. En un sistema aislado, dado el calor es siempre igual al calor absorbido o cambio de calor en el sistema es igual a cero. Si dos objetos tienen temperaturas diferentes están en contacto, la transferencia de calor se inicia entre ellos. La cantidad de calor es igual a la cantidad de calor tomada. Un objeto tiene una masa m₁, T₁ temperatura y capacidad calorífica específica c₁, dos objetos tienen masa m₂, la temperatura t₂ y capacidad calorífica específica c₂.
 Ejemplo: Encuentre la temperatura final de la mezcla, si dos taza de agua con masas m₁ = 150g y m₂ = 250g y las temperaturas T₁ = 30 º C y T₂ = 75 º Cuidado mezclan en un sistema aislado en el que no hay pérdida de calor.(cwater=1cal/g.ºC)
Ejemplo: Encuentre la temperatura final de la mezcla, si dos taza de agua con masas m₁ = 150g y m₂ = 250g y las temperaturas T₁ = 30 º C y T₂ = 75 º Cuidado mezclan en un sistema aislado en el que no hay pérdida de calor.(cwater=1cal/g.ºC)
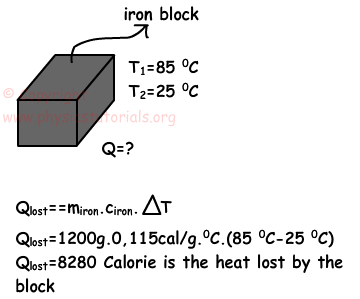
 Ejemplo: La temperatura del bloque de hierro se reduce de 85ºC a 25ºC. Si la masa del bloque es de 1,2 kg, calcular el calor perdido por el bloque. (Ciron = 0.115cal / g. º C)
Ejemplo: La temperatura del bloque de hierro se reduce de 85ºC a 25ºC. Si la masa del bloque es de 1,2 kg, calcular el calor perdido por el bloque. (Ciron = 0.115cal / g. º C)
 Ejemplo: El gráfico a continuación muestra la relación entre el calor emitido y el cambio en las temperaturas de las tres cuestiones que tengan las mismas masas. Comparar los calores específicos de estos asuntos.
Ejemplo: El gráfico a continuación muestra la relación entre el calor emitido y el cambio en las temperaturas de las tres cuestiones que tengan las mismas masas. Comparar los calores específicos de estos asuntos.
 Dado que las masas de estos asuntos son iguales, B tiene la mayor capacidad de calor específico, ya que, con la misma cantidad de calor, cambios en la temperatura de la B es menor que los otros dos asuntos. Por otra parte, A tiene la capacidad mínima de calor específico, debido a que el cambio en su temperatura con la misma cantidad de calor es mayor que los demás. Por último, la capacidad de calor específico de la C está entre A y B. Por lo tanto,
Dado que las masas de estos asuntos son iguales, B tiene la mayor capacidad de calor específico, ya que, con la misma cantidad de calor, cambios en la temperatura de la B es menor que los otros dos asuntos. Por otra parte, A tiene la capacidad mínima de calor específico, debido a que el cambio en su temperatura con la misma cantidad de calor es mayor que los demás. Por último, la capacidad de calor específico de la C está entre A y B. Por lo tanto,
cB>cC>cA
El Calor, la Temperatura y la Expansión Térmica Exámenes y Soluciones